- Qu’est-ce que l’inflammation ?
L’inflammation chronique, également connue sous le nom « d’inflammation de bas grade » ou « inflammation systémique », correspond à un dérèglement métabolique de plus en plus présent dans la population générale.
Attention cependant aux raccourcis : l’inflammation en tant que telle est un processus tout à fait naturel et nécessaire au cours duquel l’organisme se défend contre une agression extérieure. Ces éléments externes peuvent par exemple venir d’une pratique sportive intensive, d’une brulure cutanée, d’un virus ou bien d’un agent pathogène présent dans la circulation sanguine.
En temps normal, cette inflammation est dite « aigue » et dure de quelques heures à quelques jours, le temps pour l’organisme de lutter contre l’élément stressant et ainsi revenir à un état d’équilibre dit d’homéostasie. L’intensité, la durée et l’efficacité de celle-ci est régulée par la production de nombreuses molécules parmi lesquelles on retrouve les lymphocytes, les macrophages ou encore les cytokines (cf. schéma ci-dessous).
Ces cytokines régulent les mécanismes d’inflammation via la signalisation cellulaire, c’est-à-dire la capacité des cellules à communiquer entre elles et coordonner leurs activités. Elles sont produites par les cellules évoquées sur le schéma ci-dessous, à savoir les lymphocytes, les granulocytes ou encore les macrophages. On retrouve des cytokines anti-inflammatoires et pro-inflammatoires !
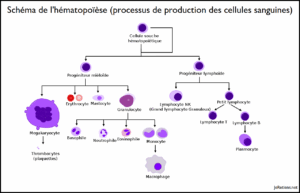
Figure 1 : Les différentes molécules impliquées dans la réponse immunitaire
- Quand l’inflammation devient chronique
Le problème survient quand l’inflammation aigue et physiologique devient chronique et donc potentiellement délétère pour le bon fonctionnement de l’organisme.
L’inflammation chronique est un phénomène le plus souvent asymptomatique et qui est retrouvé dans la plupart des maladies dites « de civilisation », qu’elles soient auto-immunes, métaboliques, cardiovasculaires ou neuro-dégénératives. Contrairement à l’inflammation aigue, elle ne se manifeste donc pas par des symptômes de douleur, de chaleur, de rougeur ou de gonflement.
L’inflammation chronique est également une caractéristique et l’une des problématiques majeures chez les personnes en situation et surpoids et/ou d’obésité ; en effet, le tissu adipeux constituant un tissu endocrine à part entière, l’accumulation de tissu adipeux favorise la production de cytokines pro-inflammatoires spécifiques que l’on appelle des adipokines. L’inflammation chronique fait donc partie intégrante de ce que l’on appelle le syndrome métabolique (1)(2). Ce syndrome est présent lorsqu’un patient présente à minima 3 des 5 critères ci-dessous :
- Augmentation tour de taille – prise de poids, notamment viscérale
- Altération profil lipidique – faibles valeurs de HDL + augmentation triglycérides
- Altération métabolisme glucidique – augmentation glycémie et baisse de la sensibilité à l’insuline des cellules cibles
- Hypertension artérielle – facteur à part entière lié à l’augmentation du risque de maladies cardio-vasculaires.
Elle constitue donc un facteur majeur de risque en matière de santé publique et un enjeu en matière de santé préventive. On retrouve également fréquemment une inflammation de bas grade en cas de dépression (3). Une méta-analyse (4) menée sur près de 14 000 patients victimes de dépression montrent que 50% d’entre eux ont des valeurs de protéine C réactive supérieures à 1mg/L et 27% supérieures à 3mg/L ! L’inflammation de bas grade contribuerait notamment à réduire la production d’une molécule essentielle au bien-être, la sérotonine. Sans rentrer trop dans le détail, l’inflammation pourrait, entre autres facteurs, réduire la conversion du tryptophane en sérotonine au profit d’une autre voie biochimique, celle de la kynurénine.
L’inflammation de bas grade peut également être retrouvée en cas de déséquilibres de la sphère digestive. En effet, il peut arriver que certaines bactéries intestinales, normalement présentes au niveau du microbiote, se mettent à proliférer. C’est ce que l’on retrouve en situation de dysbiose intestinale. Ces bactéries possèdent la capacité de produire des molécules pro-inflammatoires nommées lipopolysaccharides (LPS). Ces LPS peuvent endommager la barrière intestinale et se retrouver dans la circulation sanguine (cf. schéma ci-dessous). Lorsque cela intervient, ces LPS activent des récepteurs nommés TLR4 qui à leur tour déclenchent la production de cytokines pro-inflammatoires, dont nous reparlerons plus tard. L’activation de ces récepteurs TLR4, et subséquemment de la voie NF-κB, engendre la production de cytokines pro-inflammatoires dont nous reparlerons plus tard.
In fine, ces déséquilibres au niveau de l’écosystème intestinal peuvent à terme conduire à la prise de poids (5), à la résistance à l’insuline (6) ou encore à l’obésité (7).
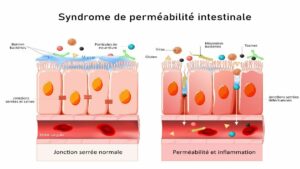
Figure 2 : Passage de LPS au travers de la barrière intestinale
Plusieurs marqueurs permettent de quantifier cette inflammation chronique. Parmi ces marqueurs, on retrouve notamment la protéine C réactive (CRP), le bilan martial et certaines cytokines pro-inflammatoires. Attardons nous d’abord en détail sur la CRP, de loin le marqueur le plus étudié dans les études scientifiques et le plus accessible en pratique courante.
- Protéine C réactive
La protéine C réactive (CRP) est une protéine fabriquée principalement par le foie (mais également par les cellules endothéliales, les macrophages ou les adipocytes) et impliquée de manière prépondérante dans la régulation de l’inflammation, qu’elle soit aigue ou chronique. Sa production est déclenchée en réponse à l’augmentation des cytokines pro-inflammatoires, principalement l’IL-6 mais également l’IL-1β (8)(9).
Dans le cas d’une inflammation aigue, la CRP s’élève fortement, pouvant atteindre des valeurs de l’ordre de 100 voire 1000mg/L. Lors d’une inflammation de bas grade, cette valeur de CRP est souvent bien plus faible, rendant le diagnostic beaucoup plus compliqué, notamment car la plupart des médecins ou professionnels de santé n’y accordent que peu d’importance. A l’heure actuelle, la plupart des laboratoires de biologie, et par extension du corps médical, considèrent qu’une CRP est dans les normes lorsque située en dessous de 5mg/L. C’est malheureusement absurde au regard des données scientifiques, voici pourquoi :
- Au-dessus de 3mg/L :
En effet, des valeurs situées au-dessus des 3mg/L sont unanimement reconnues comme étant un facteur de risque majeur de survenue de maladies cardio-vasculaires et de maladies chroniques (10)(11), potentiellement plus pertinent que le LDL-cholestérol dans le cadre des pathologies cardio-vasculaires d’après une étude parue en 2002 (12). Cette étude précise toutefois que l’idéal demeure d’utiliser les 2 marqueurs de manière conjointe plutôt que de façon isolée. L’importance de la CRP dans l’évaluation du risque cardio-vasculaire s’explique par le rôle prépondérant de l’inflammation chronique dans le processus d’athérosclérose. En effet, celui-ci n’est pas seulement une obstruction des artères causée par le dépôt de graisses. De nombreux autres facteurs, comme le stress oxydant, les triglycérides ou encore l’hypertension artérielle, contribuent à la formation de la plaque athéromateuse. A noter également que le ratio CRP/HDL serait un bon indicateur des risques cardio-vasculaires encourus par une personne (13). Ce ratio reste toutefois à utiliser en complément d’autres indicateurs comme le LDL et la présence éventuelle de comorbidités.
Une étude intéressante (14) ayant utilisé un suivi moyen de 7 ans sur 4000 personnes a montré que le risque de cancer était augmenté de 65% en cas de CRP ultrasensible (CRPUS) supérieure à 3mg/L par rapport à des personnes présentant des valeurs inférieures à 1mg/L. Le risque de maladies cardio-vasculaire était quant à lui doublé, au même titre que le risque de mortalité toutes causes confondues.
Plusieurs études (15)(16) sont également parvenues à mettre en évidence une relation plus ou moins étroite entre l’indice de masse corporelle (IMC) et les concentrations en CRPUS dans le sang ; une augmentation de l’IMC aurait ainsi tendance à engendre une augmentation des niveaux d’inflammation de bas grade. Cependant, l’IMC à lui seul ne suffit plus à caractériser la présence d’obésité chez une personne ; les spécialistes s’orientent ainsi de plus en plus vers l’utilisation du tour de taille ou du % de masse grasse, obtenus à l’aide de méthodes comme la DEXA. Ce faisant, une étude taiwanaise (17) est parvenue à démontrer que ce % de masse grasse totale était étroitement corrélé aux valeurs de CRPUS. Cela semble cohérent avec ce que nous évoquions concernant le syndrome métabolique, syndrome au sein duquel une élévation du tour de taille et une augmentation du % de masse grasse – notamment au niveau viscéral – est très fréquemment retrouvée (18).
- En-dessous de 1mg/L :
Mais alors qu’en est-il des valeurs « normales » de CRP et qui permettraient de conclure à l’absence d’un terrain inflammatoire de bas grade ?
A l’heure actuelle, il n’existe pas à ma connaissance de valeurs consensuelles permettant de définir une valeur de CRP comme « physiologique » ou au contraire « pathologique ». La branche « conventionnelle » de la médecine considère des valeurs de CRP inférieures à 5 comme normales, en dépit des risques avérés au niveau cardio-vasculaire d’une CRP durablement au-dessus de 3mg/L. A l’inverse, l’approche « fonctionnelle » ou « intégrative » considère des valeurs supérieures à 1mg/L comme étant le témoin infaillible de la présence d’une inflammation de bas grade. Entre ces deux extrêmes, autant de nuances de gris susceptibles de laisser les patients dans le flou et dans l’incompréhension.
D’un point de vue statistique, des valeurs de CRP inférieures à 1mg/L sembleraient associées à une absence de risque majeurs sur les plans métaboliques et cardiovasculaires (19). Des valeurs de CRP inférieures à 1 traduisent l’absence probable d’état inflammatoire chronique et constituent donc un élément rassurant sur la santé de l’individu. Pour autant, des valeurs basses de CRP ne sont pas considérés comme « protectrices » d’un point de vue de la santé métabolique et cardio-vasculaire : elles diminuent simplement les risques par rapport à des valeurs plus élevées. De plus, attention à ne pas surinterpréter les valeurs de CRP, celles-ci devant toujours être analysées au regard du profil global de la personne, aussi bien en ce qui concerne les autres marqueurs biologiques que les symptômes cliniques et les habitudes de vie. A noter également que, selon certains travaux (20)(21), 30 à 50% des variations interindividuelles en matière de CRP pourraient être imputées à des facteurs génétiques !
- Entre 1 et 3mg/L :
Comme évoqué précédemment, la zone située entre 1 et 3mg/L est tantôt considérée comme tout à fait normale et tantôt comme le reflet d’une inflammation à bas bruit. Alors que disent les études à ce sujet ?
Une méta-analyse chinoise (22) de 2021 nous apporte un élément de réponse : regroupant 60 études et près de 230 000 patients, cette étude suggère que chaque augmentation de 1mg/L des valeurs de CRP serait associée à une augmentation moyenne de 18% du risque de maladies cardio-vasculaires et de 7% du risque d’AVC. Une autre étude (23) de cohorte menée sur près de 28 000 patients suggère que le risque cardio-vasculaire serait même doublé pour une CRP située entre 0.5 et 1mg/L par rapport à une CRP inférieure à 0.5mg/L. En ce qui concerne le risque de diabète de type 2, celui-ci augmenterait d’en moyenne 12% (95%CI, 1.06-1.17) pour chaque augmentation de 1mg/L de la CRP (24), avec un plafond au-delà de 5mg/L. Pour ce qui est des cancers, des valeurs de CRP situées entre 1 et 3mg/L ne semblent pas clairement associées à une augmentation du risque à terme. Cependant, ces risques semblent clairement augmentés en cas de CRP au-delà de 3mg/L : c’est notamment ce que rapporte une étude Danoise (25) menée sur près de 10 000 individus suivis pendant 16 ans. Dans cette étude, des valeurs de CRP supérieures à 3mg/L étaient associées à un risque accru de développer un cancer (tous types confondus) de l’ordre de 30% (95% CI, 1.0 to 1.6).
Les résultats de ces études sont toutefois à prendre avec précaution. En effet, les risques en matière de pathologie dépendent de nombreux facteurs autres que l’inflammation, bien que celle-ci en soit probablement un élément central.
Au vu des études scientifiques mentionnées, il est cependant regrettable qu’un outil comme le SCORE-2 (genre, âge, tabac, cholestérol non HDL, pression artérielle), utilisé notamment par la société française de cardiologie, n’intègre pas la composante inflammatoire dans le calcul du risque cardio-vasculaire d’un individu donné.
- Les autres tests permettant d’évaluer l’inflammation
En plus de la CRP, il existe d’autres tests permettant d’évaluer les niveaux d’inflammation dans le corps.
Dans les prises de sang de routine, la vitesse de sédimentation (VS) peut être utilisée afin de mettre en évidence une inflammation dans l’organisme. Celle-ci a pour but d’étudier la sédimentation et le dépôt des globules rouges au fond d’un tube lorsque ceux-ci se séparent du plasma. Cette analyse est cependant assez peu précise et fiable et permet surtout de renseigner sur la présence d’une pathologie grave lorsqu’elle est très augmentée.
En suivi biologique de routine, le fibrinogène et l’électrophorèse des protéines sériques permettent également d’évaluer les niveaux d’inflammation de l’organisme, en complément de la CRP et de la VS.
Toujours sur les marqueurs de routine, le bilan martial peut s’avérer un bon indicateur d’un terrain inflammatoire : en effet, en cas d’inflammation importante, la production d’une cytokine pro-inflammatoire que l’on appelle l’interleukine-6 (IL-6) va engendrer la production d’une autre protéine, l’hepcidine. Celle-ci a pour but de bloquer les mouvements de fer intra-cellulaires en agissant sur la ferroportine. Résultat des courses : l’inflammation bloque le fer à l’intérieur des cellules, augmentant la ferritine et abaissant le fer sérique, et ce afin d’empêcher le développement d’un agent pathogène. On peut donc se retrouver en présence d’une anémie inflammatoire ou le fer piégé à l’intérieur des cellules empêche la formation de nouveaux globules rouges.
La présence d’un état inflammatoire aigue ou chronique peut aussi être mesuré à l’aide des cytokines pro et anti-inflammatoires. Parmi les cytokines pro-inflammatoires les plus connues et les plus utilisées dans les études, on retrouve notamment l’IL-6, le TNF-α, l’IFN-ϒ ou encore l’IL-1β. Certaines cytokines possèdent qui plus est l’avantage d’être spécifiques à une ou plusieurs pathologies. Malheureusement, ces tests ne sont pas disponibles en biologie de routine et restent donc cantonnés à un usage scientifique, eu égard à leurs coûts importants et à certaines limitations méthodologiques.
Enfin, mentionnons pour terminer le cas d’un nouveau marqueur, le suPAR (Soluble urokinase plasminogen activator receptor). Sans rentrer dans trop de détails, ce marqueur permettrait d’évaluer la présence d’inflammation chronique/de bas grade chez un patient, ceci en étant beaucoup moins impacté que la CRP par les variations inflammatoires aigues de l’organisme (26)(27).
Il semblerait qui plus est que le suPAR soit un marqueur fiable et précis pour prédire les risques de mortalité toutes causes confondues d’un individu (28). Pour autant, il n’est absolument pas spécifique à une ou plusieurs pathologies et encore que très peu disponible en biologie de routine. Certains laboratoires le proposent mais cela reste relativement rare et donc à voir au cas par cas.
- Références
- Devaraj, S., Singh, U., & Jialal, I. (2009). Human C-reactive protein and the metabolic syndrome. Current Opinion in Lipidology, 20, 182–189. https://doi.org/10.1097/mol.0b013e32832ac03e.
- Mirhafez, S., Ebrahimi, M., Karimian, M., Avan, A., Tayefi, M., Heidari-Bakavoli, A., Parizadeh, M., Moohebati, M., Azarpazhooh, M., Esmaily, H., Nematy, M., Safarian, M., Ferns, G., & Ghayour-Mobarhan, M. (2016). Serum high-sensitivity C-reactive protein as a biomarker in patients with metabolic syndrome: evidence-based study with 7284 subjects. European Journal of Clinical Nutrition, 70, 1298-1304. https://doi.org/10.1038/ejcn.2016.111.
- Osimo, E., Baxter, L., Lewis, G., Jones, P., & Khandaker, G. (2019). Prevalence of low-grade inflammation in depression: a systematic review and meta-analysis of CRP levels. Psychological Medicine, 49, 1958 – 1970. https://doi.org/10.1017/s0033291719001454.
- Beurel, E., Toups, M., & Nemeroff, C. (2020). The Bidirectional Relationship of Depression and Inflammation: Double Trouble. Neuron, 107, 234-256. https://doi.org/10.1016/j.neuron.2020.06.002.
- Amabebe, E., Robert, F., Agbalalah, T., & Orubu, E. (2020). Microbial dysbiosis-induced obesity: role of gut microbiota in homoeostasis of energy metabolism. British Journal of Nutrition, 123, 1127 – 1137. https://doi.org/10.1017/s0007114520000380.
- Saad, M., Santos, A., & Prada, P. (2016). Linking Gut Microbiota and Inflammation to Obesity and Insulin Resistance.. Physiology, 31 4, 283-93 . https://doi.org/10.1152/physiol.00041.2015.
- Cheng, Z., Zhang, L., Yang, L., & Chu, H. (2022). The critical role of gut microbiota in obesity. Frontiers in Endocrinology, 13. https://doi.org/10.3389/fendo.2022.1025706.
- Sproston, N. R., & Ashworth, J. J. (2018). Role of C-Reactive Protein at Sites of Inflammation and Infection. Frontiers in immunology, 9, 754. https://doi.org/10.3389/fimmu.2018.00754
- Boras, E., Slevin, M., Alexander, M. Y., Aljohi, A., Gilmore, W., Ashworth, J., Krupinski, J., Potempa, L. A., Al Abdulkareem, I., Elobeid, A., & Matou-Nasri, S. (2014). Monomeric C-reactive protein and Notch-3 co-operatively increase angiogenesis through PI3K signalling pathway. Cytokine, 69(2), 165–179. https://doi.org/10.1016/j.cyto.2014.05.027
- Bassuk, S., Rifai, N., & Ridker, P. (2004). High-sensitivity C-reactive protein: clinical importance.. Current problems in cardiology, 29 8, 439-93 . https://doi.org/10.1016/S0146-2806(04)00074-X.
- Ridker, P., Macfadyen, J., Glynn, R., Bradwin, G., Hasan, A., & Rifai, N. (2020). Comparison of interleukin-6, C-reactive protein, and low-density lipoprotein cholesterol as biomarkers of residual risk in contemporary practice: secondary analyses from the Cardiovascular Inflammation Reduction Trial.. European heart journal. https://doi.org/10.1093/eurheartj/ehaa160.
- Ridker, P. M., Rifai, N., Rose, L., Buring, J. E., & Cook, N. R. (2002). Comparison of C-reactive protein and low-density lipoprotein cholesterol levels in the prediction of first cardiovascular events. The New England journal of medicine, 347(20), 1557–1565. https://doi.org/10.1056/NEJMoa021993
- Gao, Y., Wang, M., Wang, R., Jiang, J., Hu, Y., Wang, W., Wang, Y., & Li, H. (2024). The predictive value of the hs-CRP/HDL-C ratio, an inflammation-lipid composite marker, for cardiovascular disease in middle-aged and elderly people: evidence from a large national cohort study. Lipids in health and disease, 23(1), 66. https://doi.org/10.1186/s12944-024-02055-7
- Koenig, W., Khuseyinova, N., Baumert, J., & Meisinger, C. (2008). Prospective study of high-sensitivity C-reactive protein as a determinant of mortality: results from the MONICA/KORA Augsburg Cohort Study, 1984-1998. Clinical chemistry, 54(2), 335–342. https://doi.org/10.1373/clinchem.2007.100271
- Huffman, F. G., Whisner, S., Zarini, G. G., & Nath, S. (2010). Waist circumference and BMI in relation to serum high sensitivity C-reactive protein (hs-CRP) in Cuban Americans with and without type 2 diabetes. International journal of environmental research and public health, 7(3), 842–852. https://doi.org/10.3390/ijerph7030842
- Aydin, M., Dumlu, T., Alemdar, R., Kayapinar, O., Celbek, G., Karabacak, A., Turker, Y., Kaya, H., Ertas, F., & Atilgan, Z. (2012). Correlation between the body fat composition and high sensitive C-reactive protein in Turkish adults. Endocrine regulations, 46(3), 147–152. https://doi.org/10.4149/endo_2012_03_147
- Lin, C. C., Kardia, S. L., Li, C. I., Liu, C. S., Lai, M. M., Lin, W. Y., Chang, P. C., Lee, Y. D., Chen, C. C., Lin, C. H., Yang, C. W., Hsiao, C. Y., Chen, W., & Li, T. C. (2010). The relationship of high sensitivity C-reactive protein to percent body fat mass, body mass index, waist-to-hip ratio, and waist circumference in a Taiwanese population. BMC public health, 10, 579. https://doi.org/10.1186/1471-2458-10-579
- Despres, J., & Lemieux, I. (2006). Abdominal obesity and metabolic syndrome. Nature, 444, 881-887. https://doi.org/10.1038/nature05488.
- Fu, Y., Wu, Y., & Liu, E. (2020). C-reactive protein and cardiovascular disease: From animal studies to the clinic (Review). Experimental and Therapeutic Medicine, 20, 1211 – 1219. https://doi.org/10.3892/etm.2020.8840.
- Sas, A., Vaez, A., Jamshidi, Y., Nolte, I., Kamali, Z., Spector, T., Riese, H., & Snieder, H. (2017). Genetic and environmental influences on stability and change in baseline levels of C-reactive protein: A longitudinal twin study.. Atherosclerosis, 265, 172-178 . https://doi.org/10.1016/j.atherosclerosis.2017.08.008.
- Best, L., Balakrishnan, P., Cole, S., Haack, K., Kocarnik, J., Pankratz, N., Anderson, M., Franceschini, N., Howard, B., Howard, B., Lee, E., North, K., Umans, J., Umans, J., Yracheta, J., Navas-Acien, A., & Voruganti, V. (2019). Genetic analysis of hsCRP in American Indians: The Strong Heart Family Study. PLoS ONE, 14. https://doi.org/10.1371/journal.pone.0223574.
- Yang, X., Zhang, D., Zhao, Y., Liu, D., Li, Q., Guo, C., Tian, G., Han, M., Qie, R., Huang, S., Zhou, Q., Feng, Y., Wu, X., Zhang, Y., Li, Y., Wu, Y., Cheng, C., Hu, D., & Sun, L. (2021). Association between serum level of C-reactive protein and risk of cardiovascular events based on cohort studies. Journal of Human Hypertension, 35, 1149 – 1158. https://doi.org/10.1038/s41371-021-00546-z.
- Ridker, P., & Cook, N. (2004). Clinical Usefulness of Very High and Very Low Levels of C-Reactive Protein Across the Full Range of Framingham Risk Scores. Circulation: Journal of the American Heart Association, 109, 1955-1959. https://doi.org/10.1161/01.cir.0000125690.80303.a8.
- Chien, K., Hsu, J., & Tsai, S. (2024). ASSOCIATION OF C-REACTIVE PROTEIN LEVEL WITH THE RISK OF TYPE 2 DIABETES: SYSTEMATIC REVIEW AND A DOSE-RESPONSE META-ANALYSIS. Journal of Hypertension, 42, e278. https://doi.org/10.1097/01.hjh.0001022376.56216.0b.
- Allin, K., Bojesen, S., & Nordestgaard, B. (2009). Baseline C-reactive protein is associated with incident cancer and survival in patients with cancer.. Journal of clinical oncology : official journal of the American Society of Clinical Oncology, 27 13, 2217-24 . https://doi.org/10.1200/jco.2008.19.8440.
- Rasmussen, L., Petersen, J., & Eugen-Olsen, J. (2021). Soluble Urokinase Plasminogen Activator Receptor (suPAR) as a Biomarker of Systemic Chronic Inflammation. Frontiers in Immunology, 12. https://doi.org/10.3389/fimmu.2021.780641.
- Rasmussen, L., Caspi, A., Ambler, A., Danese, A., Elliott, M., Eugen-Olsen, J., Hariri, A., Harrington, H., Houts, R., Poulton, R., Ramrakha, S., Sugden, K., Williams, B., & Moffitt, T. (2020). Association Between Elevated suPAR, a New Biomarker of Inflammation, and Accelerated Aging. The Journals of Gerontology Series A: Biological Sciences and Medical Sciences, 76, 318 – 327. https://doi.org/10.1093/gerona/glaa178.
- Petersen, J., Kallemose, T., Barton, K., Caspi, A., & Rasmussen, L. (2020). Soluble urokinase plasminogen activator receptor (suPAR) as a prognostic marker of mortality in healthy, general and patient populations: protocol for a systematic review and meta-analysis. BMJ Open, 10. https://doi.org/10.1136/bmjopen-2019-036125.